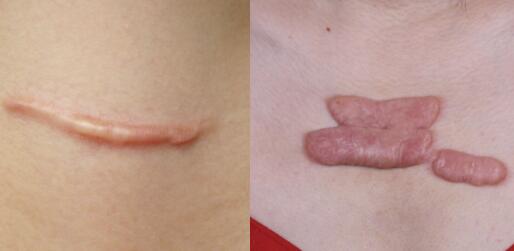
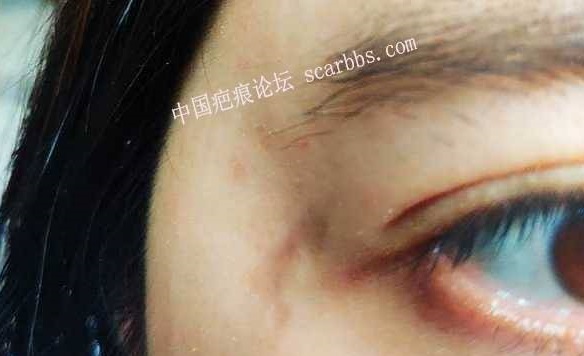
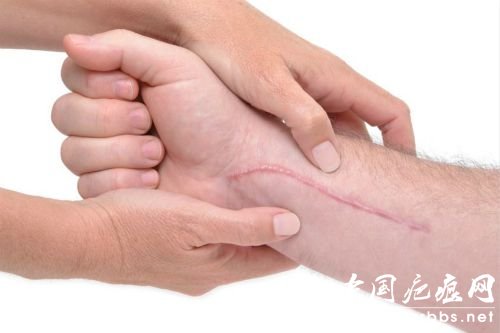
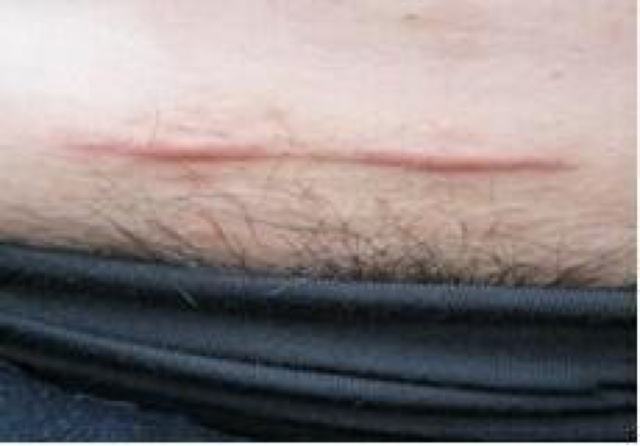
伤口愈合通常伴随着疤痕的形成。迪士尼电影《狮子王》中,木法沙的弟弟刀疤眼睛上的疤痕应该就是争斗受伤后的留下的印记。伤疤可能是少年追梦的勋章,但更多的时候,伤疤的存在可能会影响人们面容的美观、组织和关节生长以及造成皮肤等组织永久性功能丧失,而全世界疤痕修复的花费都相当高并且这种修复并非易事【1】。因此,如何在伤口愈合的同时又不产生疤痕,是科学家以及医生在皮肤修复方面研究的重要课题。
为此,美国斯坦福大学医学院Michael T. Longaker研究组与Geoffrey C. Gurtner研究组合作Science发文题为Preventing Engrailed-1 activation in fibroblasts yields wound regeneration without scarring,揭开了再生过程中不产生疤痕的新机制。

疤痕与正常未受伤的皮肤有三个不同之处:1)它们缺乏毛囊、皮脂腺和其他真皮附属物;2)它们含有致密、平行的细胞外基质纤维,而不是未受伤皮肤中规则的“筐篮编织”结构;3)由于基质结构的改变,它们缺乏皮肤正常的弹性和强度【2】。因此,想要阻止疤痕产生则需要确保再生的组织具有与正常未受伤皮肤相似的特征。
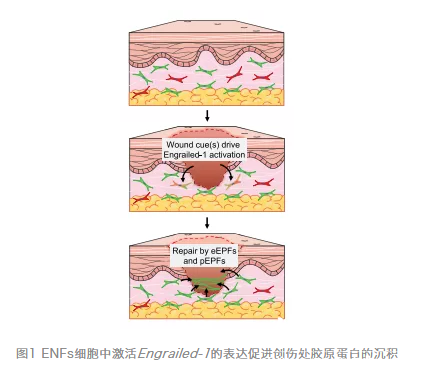
疤痕形成过程中会有Engrailed-1(En1)成纤维谱系的参与。而这其中主要包括两种成纤维细胞谱系:表达En1的谱系(En1 lineage-positive fibroblasts,EPFs)以及不表达En1的谱系(En1 lineage-negative fibroblasts,ENFs)【3】。表达En1的成纤维细胞在子宫内正常发育时出现。这些细胞及其后代被称为胚胎En1表达成纤维细胞简称为eEPFs,在出生后稳态皮肤中停止表达En1,而伤口位置中主要会存在 EPFs【3】。因此,作者们想要知道疤痕处EPFs成纤维细胞是否单纯来源于未受伤皮肤中现存的EPFs的扩增还是由于ENFs在伤口激活处转化了EPFs。
为了对该问题进行解析,作者们首先想对伤口处的成纤维细胞谱系进行分类。作者们通过细胞分选,然后将ENFs或EPFs移植到野生型小鼠真皮背侧,然后将移植的皮肤进行损伤。伤口愈合后,进行伤口疤痕和周围皮肤的组织进行收集并进行组织学分析。在未受伤的皮肤内,所有移植的成纤维细胞都表现出静息的、细长的形态。作者们发现,ENFs移植到未受伤皮肤处后,该出只有ENFs细胞存在;而在ENF移植的受伤处皮肤处,则出现了显著的EPFs细胞激活的形态,这与移植EPFs并进行受伤处理的真皮处非常相似。先前的研究中发现,EPFs中存特异的胶原蛋白沉积。通过对I型胶原蛋白的免疫染色,作者们的确发现受伤处的皮肤转变成了EPFs类似的细胞,显著表达I型胶原蛋白。进一步地,作者们确认了创伤移植ENFs中En1被激活,伤口处出现明显的ENF到EPF的过渡现象。
细胞表达整合素(Integrins)耦联粘着斑激酶(Focal adhesion kinase,FAK)对环境机械力信号进行感应,最终通过Rho/Rho相关蛋白激酶信号通路(Rho/Rho-associated protein kinase,ROCK)影响转录【4】,伤口张力的增加会增加成纤维细胞的促纤维化基因表达。作者们提出了一个假设,机械力的信号可能会激活ENFs表达En1,由此促进ENFs到EPFs的转变。为了对该假设进行检验,作者们分别将ENFs细胞培养在高硬度的培养基、高硬度的培养基加ROCK信号通路抑制剂以及低硬度培养基上。作者们发现伤口愈合后,高硬度培养基上ENFs细胞中En1的表达被显著激活,而在低硬度的凝胶中培养的ENFs细胞则未能激活En1的表达。机械刺激后,机械转导的最终转录效应子YAP转位到细胞核,激活增殖和迁移相关基因【5】。作者们发现ENFs成纤维细胞会快速激活YAP信号通路,并且出现高度的核滞留YAP信号。而在大多数的EPFs中则没有显著的YAP核定位的出现。该结果说明YAP机械信号转导途径在ENF到EPF的转变过程中发挥着关键性作用。
最后,作者们使用YAP化学抑制剂维替泊芬(Verteporfin)和转基因抑制机械转导信号通路对伤口愈合过程中En1的表达进行调节。通过RNA测序、定量组织病理学比较和机械强度测试等实验手段,将伤口处与未受伤的皮肤和疤痕处皮肤进行比较。作者们确认YAP的敲除会关闭En1的激活,促进ENF介导的伤口再生。而且YAP的抑制诱导正常皮肤超微结构的恢复。因此,这些结果说明ENFs响应伤口处的机械信号从而激活En1,促进转化成为EPFs导致疤痕的产生,而抑制YAP则有可能成为解决这一问题新方法。

总的来说,该工作发现在伤口再生过程中En-1不表达的成纤维细胞谱系会转化为表达En-1的细胞谱系,促进伤口修复但是会导致疤痕的产生。如果在此过程中机械信号驱动的纤维化过程可以被阻止,哺乳动物皮肤中ENFs保留的皮肤再生能力可以对伤口进行修复,同时也可以防止疤痕组织的产生(图2)。这一发现可能会为每年数以千万计的疤痕患者提供重要的治疗参考意义,早日达到“天下无疤”这一目标。
参考文献:
1 Gurtner, G. C., Werner, S., Barrandon, Y. & Longaker, M. T. Wound repair and regeneration. Nature453, 314-321, doi:10.1038/nature07039 (2008).
2 Mascharak, S., desJardins-Park, H. E. & Longaker, M. T. Fibroblast Heterogeneity in Wound Healing: Hurdles to Clinical Translation. Trends in molecular medicine 26, 1101-1106, doi:10.1016/j.molmed.2020.07.008 (2020).
3 Rinkevich, Y. et al. Skin fibrosis. Identification and isolation of a dermal lineage with intrinsic fibrogenic potential. Science (New York, N.Y.) 348, aaa2151, doi:10.1126/science.aaa2151 (2015).
4 Provenzano, P. P. & Keely, P. J. Mechanical signaling through the cytoskeleton regulates cell proliferation by coordinated focal adhesion and Rho GTPase signaling. Journal of cell science 124, 1195-1205, doi:10.1242/jcs.067009 (2011).
5 Panciera, T., Azzolin, L., Cordenonsi, M. & Piccolo, S. Mechanobiology of YAP and TAZ in physiology and disease. Nature reviews. Molecular cell biology 18, 758-770, doi:10.1038/nrm.2017.87 (2017).
推荐阅读:更多疤痕案例,请关注疤痕论坛https://www.scarbbs.com/
声明:转载公众号“BioArt”,如侵权,请致电:400-8940-678
- 上一篇:受伤留疤 不等同于瘢痕体质
- 下一篇:瘢痕疙瘩放射治疗的那些事儿